科研进展
彭俊平团队在淋球菌耐药检测技术研究方面取得新进展
2025年8月1日,我所彭俊平团队在《Analytical Chemistry》在线发表了题为“Development of a CRISPR/Cas-Based Detection Platform for Tracking Decreased Susceptibility to Cephalosporins in Neisseria gonorrhoeae”的研究论文。
淋病已成为日益严峻的公共卫生挑战,淋球菌抗微生物药物耐药性的快速演变给临床治疗带来严峻考验,特别是头孢菌素耐药分离株的不断涌现,严重影响了淋病的有效防治,因此被WHO列入需要研发抗菌药物的优先细菌清单(2017、2024)。目前常规检测方法存在耗时长、流程复杂等问题,难以满足淋球菌早期筛查和耐药菌株及时监测的临床需求。彭俊平团队长期致力于病原体检测技术研究,基于纳米孔测序(Clin Chem, 2021; Sci China Life Sci, 2024)、核酸质谱(J Antimicrob Chemoth, 2020a)、高分辨率熔解曲线(J Mol Diagn, 2020,J Antimicrob Chemoth, 2020b; Antimicrob Agents Chemother,2022, 2024; Int J Antimicrob Agents, 2023)、基因编辑(Chem Eng J, 2024)等技术构建高效的淋球菌耐药监测技术体系,为提升检测、监测水平提供有力工具。
本研究中,彭俊平团队成功研发了一种集成RPA-CRISPR/Cas12a的多重检测分析技术(MIRCA),用于监测全球关注的淋球菌FC428耐药克隆,同时发现对头孢菌素敏感性降低的淋球菌。MIRCA技术可在40分钟内实现淋球菌的鉴别和重要耐药相关突变位点(penA-375-377, penA-A311V, penA-A501V/T)的检测,并具备良好的特异性和灵敏度(10-20拷贝/反应)。临床评估结果显示,MIRCA 与 qPCR 方法在淋球菌鉴定方面一致率达到 100%;与 Sanger 测序相比,MIRCA 对马赛克结构的检测一致率为 99.17%;对 FC428克隆相关菌株的检测准确率达 100%;对 penA-A501 突变(A501V/A501T)的检测一致率为 98.33%。为推动MIRCA在低资源地区使用实现淋球菌的及时检测,本研究创新性地将RPA-CRISPR技术与3D打印微流控芯片相结合,实现微流控芯片平台与液体体系的检测结果完全一致,准确率达到100%。
MIRCA技术不仅具备快速、精准的检测优势,还具有经济高效的特点。该技术与微流控芯片的集成,提供了一种成本低廉且用户友好的诊断方案,为资源有限地区的即时检测提供了重要工具。该技术的应用将提升淋病耐药性监测的效率,助力临床及时诊断和治疗决策,同时为公共卫生监测和抗菌药物管理提供有力支持。该技术也为其他传染病的快速检测与耐药性监测提供了可借鉴的技术范式,具有广阔的应用前景。
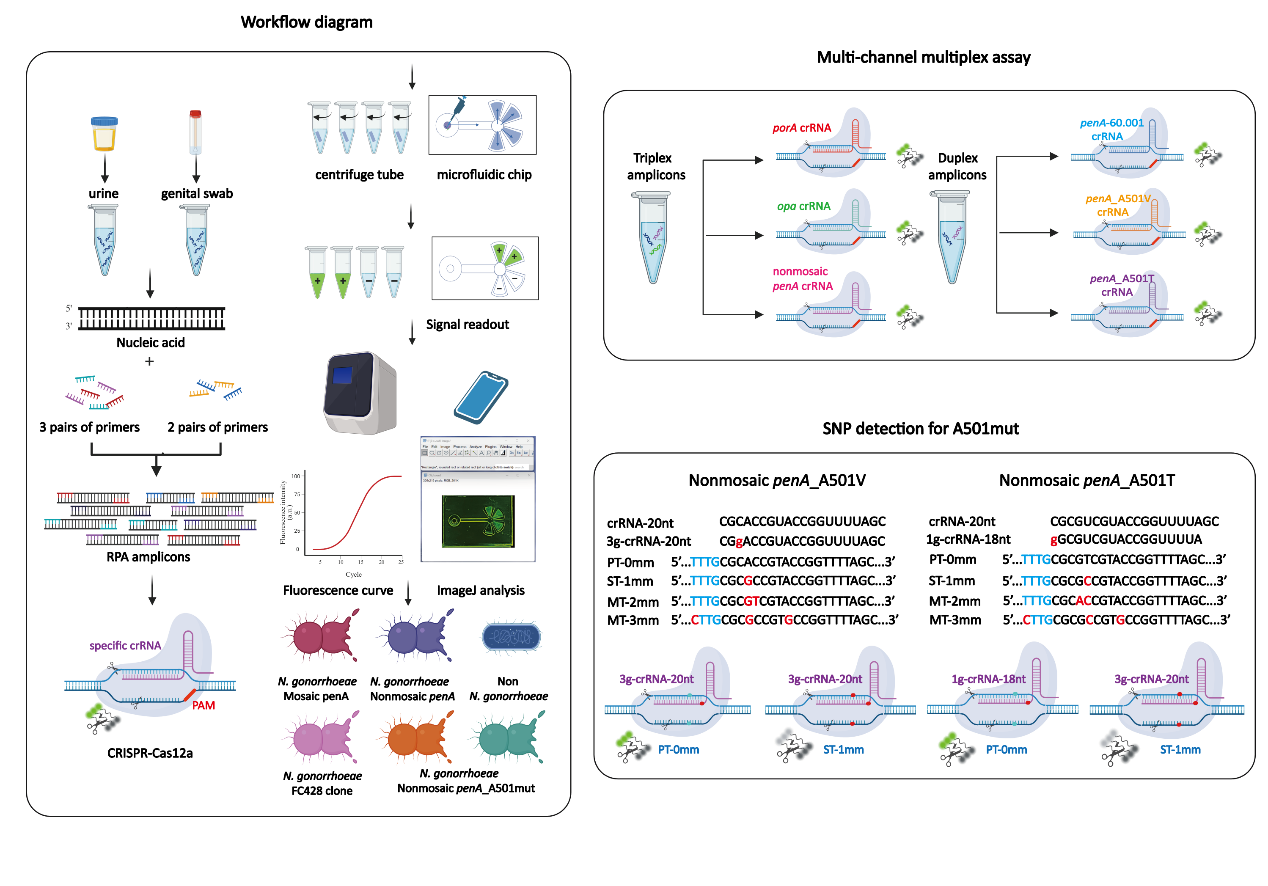
图.RPA-CRISPR/Cas12a多重检测分析技术检测淋球菌的示意图
研究得到了中国医学科学院医学与健康科技创新工程(2021-I2M-1-038和2023-I2M-2-001)、中国医学科学院中央级公益性科研院所基本科研业务费专项资金项目(2019PT310029、2023-PT310-04)等项目的支持。中国医学科学院病原生物学研究所彭俊平研究员为本文的通讯作者,博士生赵子渊为本文的第一作者。
